病気、患者、医療現場に向き合う薬学基礎研究
薬学研究は薬を武器として病気に立ち向かう研究領域です。本分野では、分子生物学の知識と技術、そして薬物動態の定量解析とシステムズバイオロジーを融合し駆使した薬学研究をおこないます。「なぜ薬学で研究をおこなわなければならないのか?」この問いに対する答えを持ちながら、薬という視点から最終的に患者、国民の利益(=ライフイノベーション)として応用できる研究を行っていきます。その一つとして、最新質量分析によるタンパク質基礎化学を応用し次世代のがん個別化治療と早期診断を実現することを目指しています。
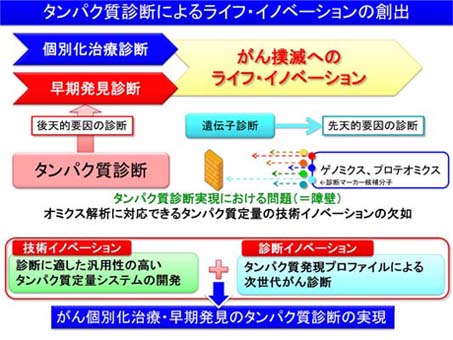
独自技術開発:質量分析による新しいタンパク質の定量システムの開発
タンパク質は生命現象を司る中心的役割を果たす分子であるため、その検出、定量技術は生命科学の根幹技術です。抗体による高感度、特異的なタンパク質検出法は生命科学の進歩に大きく貢献してきましたが、タンパク質検出は抗体へ大きく依存しており、抗体の限界によるタンパク質科学の限界を多くの生命科学者が感じています。特にゲノミクスやプロテオミクスによる網羅的解析が可能となると同定したバイオマーカー候補分子に対する抗体の有無や抗体調製の困難さが解析全体のボトルネックとなっています。
本分野では、大槻らが独自に開発した質量分析によるタンパク質定量システムの開発を分子生物学の技術を駆使して実施します。本法では配列情報のみからタンパク質定量系を構築できるだけではなく、質量に基づき極めて特異性の高い定量系を実現しています。技術詳細は先端技術大賞HPに掲載されている論文をお読み下さい。
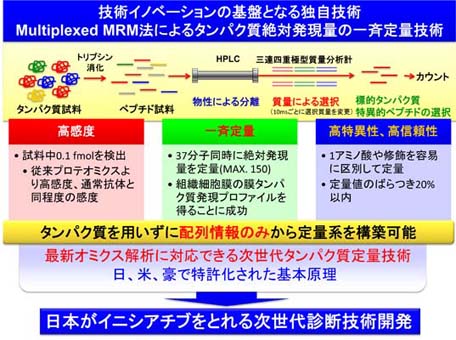
質量分析の技術は、生命科学領域だけではなく創薬分野において必須の技術となりつつあります。本分野では、異なる特徴を持つ5台の最新質量分析装置を設置し、研究にフルに活用します。質量分析の基礎から応用まで習得することができます。
質量分析装置はカスタマイズによっていろいろな応用が可能です。メカ好き、コンピュータ好きの学生大募集中です。
次世代個別化治療:タンパク質診断によるがん個別化治療の実現
近年、がん治療において分子標的薬が開発され、そのめざましい効果が注目されています。しかし、その激しい副作用や高額な医療費という問題もかかえています。従って、効果が期待できる患者を選択できる診断と適応症例の拡大が急務です。治療個別化診断は、主に遺伝子レベルでの診断開発が進行し、変異遺伝子の検出による選択に成功しています。しかし、その診断は一部の有効患者の検出を実現しているのみであり、多くの潜在的な有効患者は恩恵にあずかることができないでいます。
分子標的薬は標的タンパク質の生理活性と相関性の高い指標が有効患者の検出に有効であると考えられます。標的タンパク質の多くが膜タンパク質であるため、遺伝子発現がタンパク質発現や活性と極めて相関性が悪いことが遺伝子診断の限界です。すなわち、活性と相関性の高い細胞膜上の標的タンパク質発現量及び変異タンパク質の発現量を計測することが、最も汎用性の高く優れた診断法になると期待されます。さらに、複数の標的タンパク質発現量をプロファイル解析することが可能であれば、プロファイル情報を基にして新たな分子標的薬の適応が可能となり、がん患者のQuality of Lifeの劇的な改善の実現が期待されます。そこで、独自の質量分析によるタンパク質定量システムを用い、分子標的薬の標的タンパク質発現量によるがん化学療法の個別化治療の実現を目指します。
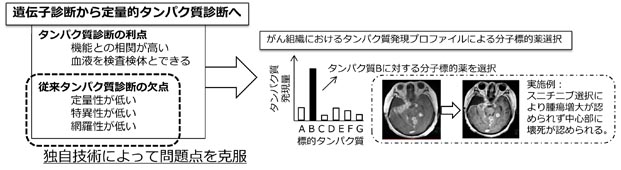
金沢大学病院 濱田教授・中田講師との共同研究において化学療法は無効で再発を頻発していた悪性髄膜腫患者に対し、がん組織検体の標的タンパク質発現量を測定し、その発現量を基にした分子標的薬の適応拡大治療を、倫理委員会の承認の元、実施しました。2週間でがん組織の壊死が認められ、1ヶ月後においてもがん組織の腫瘍の増大が認められない驚くべき結果を得ました。現在、タンパクし発現量を基にした個別化治療は例数を増やしています。
Yoshikawa et al. Recurrent anaplastic meningioma treated by sunitinib based on results from quantitative proteomics.Neuropathol Appl Neurobiol.(2011)
臨床の現場との共同研究は基礎研究とは異なる新しい発見と緊張感があり、現場からの切実なニーズが大きなモチベーションとなります。基礎研究と臨床現場を結びつける馬力と責任感のある学生を大募集中です。
次世代がん診断:タンパク質診断によるがん早期診断の実現
有効な個別化治療のためには、がんの早期診断が不可欠です。人間ドックによる血中腫瘍マーカー検査やがん検診の普及が国家レベルでおこなわれています。しかし、血中腫瘍マーカーは擬陽性などのためその効果を疑問視する声が多くあり、また、がん検診は患者への様々値面での負担を強いるため検診率は約20%にとどまっています。このような負のスパイラルによって早期診断の実現は厳しい現状にあります。
この現状を打破するためには、患者の負担軽減及び信頼性の向上が必須です。遺伝子診断は網羅的かつ簡便でありますが血液検体ではdegradationのため、応用が極めて限定的です。一方で、独自のタンパク質定量技術の応用によって、微量血液から一般的な診断分子と血中腫瘍マーカーの一斉定量を実現できれば、患者の負担を著しく低減することが可能なだけではなく、多数の腫瘍マーカーによる総合診断によるより確度の高い診断が可能になります。
早期診断を目指し様々なゲノミクスやプロテオミクスの研究が進行しています。ゲノミクスやプロテオミクスにおいてバイオマーカーの候補分子を多数同定したとしても、次の段階で候補分子を絞り込み、バイオマーカーを同定するためには個別のタンパク質定量系が必要となります。定量系が全くないタンパク質は、抗体を作成しなければなりません。我々の独自技術は、このような現在のオミクス解析が抱えるボトルネックを克服することが可能です。そこで、国内外の研究者と共同研究を行い、がん早期診断のバイオマーカー探索に留まらず、候補分子の定量系の構築、さらにマーカーとしての検証実験を技術開発と共に積極的に進めています。
マーカー検証は、がん診断の実用化に直結します。基礎研究成果の医療への実用化を切望する意欲のある学生を大募集中です。
上記の様な研究は、地道な基礎研究を基盤とした応用研究として成り立ちます。つまり、本分野では基礎研究も重視して行っていきます。その際にも、「薬学研究として医療現場にどのような応用ができるのか」というビジョンを持ちながら基礎研究を実施します。
研究内容に興味のある方は大槻(sohtsuki(a)ohtsuki-lab.jp)までご連絡下さい。 (a)を@に変換して下さい。







